האם קדימהסטם תמצא תרופה ל־ALS לפני שייגמר לה הכסף?
מפתחת התרופות שרפה 100 מיליון שקל מאז הנפקתה ובסוף 2016 נותרו בקופתה רק 2.5 מיליון שקל. כעת היא מקווה שאישור תקדימי שהעניק ה־FDA לשיווק תרופה שנוסתה מחוץ לארה"ב יאפשר לה לבקש אישור דומה על סמך ניסוי שתערוך בהדסה
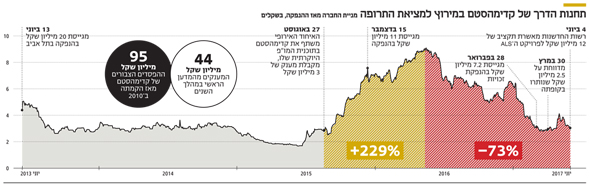
הודעתה של עינת צפריר שלשום כי התפטרותה מדירקטוריון קדימהסטם נבעה ממצבה הפיננסי הקשה של מפתחת התרופה למחלת ניוון השרירים (ALS), ומהחשש שהחברה עלולה להפסיק את פעילותה בקרוב גרמה לכך המניית החברה השילה אתמול 17% מערכה בבורסה של תל אביב. ואכן, המצב הפיננסי של החברה העוסקת בפיתוח תרופות מבוססות תאי גזע אינו מזהיר. קדימהסטם, שהוקמה ב־2010, שרפה כמעט 100 מיליון שקל מאז הפיכתה לציבורית ביוני 2013, רובו כסף ציבורי. כבר בהנפקה גררה החברה הפסד מצטבר של 27 מיליון שקל, ומאז ועד היום מצורפת לדו"חותיה הערת עסק חי. גם השווי שלה בעת ההנפקה עמד על כ־70 מיליון שקל, קרוב לשווייה הנוכחי שעומד על 68 מיליון שקל. את 2016 היא סיימה עם הפסד של 20 מיליון שקל ועם 2.5 מיליון שקל בלבד בקופת המזומנים המצטמקת.
התרופה שעשתה היסטוריה
אלא שביומיים שעברו מאז התפטרותה של צפריר, קדימהסטם הצליחה לקבל מענק של 12 מיליון שקל מהרשות לחדשנות במשרד הכלכלה, ודיווחה כי בעלי השליטה ובעלי העניין בחברה הביעו נכונות וכוונה להמשיך ולתמוך בה לצורך המשך פעילותה השוטפת. האופטימיות של קדימהסטם נובעת מהתפתחות מפתיעה בשוק הפארמה הגלובלי, שעשויה לסלול לקדימהסטם את הדרך לקבלת אישור של רשות המזון והתרופות האמריקאי (FDA). בתחילת מאי תרופה אחת ל־ALS עשתה היסטוריה כאשר קיבלה אישור של ה־FDA שלראשונה הסתמך על ניסויים שנעשו מחוץ לארה"ב. המדובר ברדיקווה (Radicava), המיוצרת על ידי Mitsubishi Tanabe Pharma שנסחרת בבורסה של טוקיו. קבלת אישור ה־FDA לתרופה שמשווקת כבר כמה שנים ביפן ובקוריאה הדרומית, הזניקה את מניית החברה היפנית לשיא וגררה פרסומים רבים ברחבי העולם.
ה־ALS תוקפת תאי עצב שמפעילים שרירים וגורמת לשיתוק הדרגתי של הגוף, אבל אינה פוגעת ביכולות השכליות של החולים שתוחלת החיים שלהם נעה בין שלוש לחמש שנים מרגע האבחון. המחלה קרויה גם מחלת לו גריג על שם שחקן בייסבול אמריקאי מפורסם שחלה בה. בין החולים המפורסמים ב־ALS בארץ ובעולם גם הפיזיקאי סטיבן הוקינג וגם סטיבן הילנבורג, יוצר הסדרה בוב ספוג, שניהם עדיין בחיים, והתעשיין דב לאוטמן שנפטר ב־2013 ושדר הטלוויזיה מאיר איינשטיין שחשף השנה כי לקה ב־ALS ונפטר זמן קצר לאחר מכן.
עד להודעה של Mitsubishi, שווקה בארה"ב במשך 22 שנה תרופה אחת בלבד (Rilutek) שמאריכה את חיי החולים ב־ALS בעד שלושה חודשים. לפי הערכה, קיימים כ־450 אלף חולים במחלה בכל העולם, כאשר עלות הטיפול בחולים בארה"ב לבדה עומדת על 6 מיליארד דולר בשנה. בשל היעדר תרופות, עיקר הטיפול בחולים מתמקד בפיזיותרפיה, ריפוי בעיסוק, תרפיה דיבורית ואמצעים מלאכותיים להארכת החיים.
הכיוון החדש של ה־FDA
התרופה היפנית ניתנת באמצעות עירוי לווריד. אישור ה־FDA שאותו קיבלה מסתמך על תוצאות הניסוי הקליני שלב 3 שבו השתתפו 137 מטופלים בשלבי מחלה התחלתיים יחסית עם תפקודי נשימה תקינים. התרופה הצליחה להציג שיפור מתון במצב החולים במדד העיקרי שבו נבדק תפקוד החולים (ALSFRS).
לפי אתר איגוד ה־ALS העולמי מחיר עירוי בודד של רדיקווה מוערך באלף דולר וטיפול שנתי מוערך ב־150 אלף דולר. אישור ה־FDA ניתן לתרופה חרף האפקטיביות המוגבלת ותופעות הלוואי שלה שכוללים כאבי ראש ושטפי דם, וחרף העובדה שהתרופה עדיין לא הוכחה כמתאימה לחולים במצב מתקדם ככל הנראה כתוצאה מהצורך הגדול בפתרונות לחולים הקשים, הנותרים ללא מענה.
ג'ייסון קולברט, ראש מחלקת מחקר של בנק ההשקעות האמריקאי Maxim Group, המסקר את תחום הטיפולים ב־ALS, ציין לאחרונה כי הוא מופתע מהאישור החריג שקיבלה הרדיקווה, מאחר שלדבריו, מדובר בתרופה המבוססת על מנגנון פעולה ידוע ומוכר, שאינו ייחודי למחלת ה־ALS.
עם זאת, קולברט, כמו מומחים אחרים בתחום הפארמה בארה"ב, מאמינים כי אישור ה־FDA סולל את הדרך לתרופות חדשניות יותר, המבוססות על מנגנוני פעולה שהוכחו יעילים יותר בתחום ה־ALS, וכי מדובר בכיוון חדש של ה־FDA להענקת הקלות לתרופות חדשות עם דגש על תרופות יתום ותרופות למחלות חשוכות מרפא ללא מענה בשוק.
בכמה ארצות במזרח הרחוק כבר מונהגות תקנות המאפשרות לחברות פארמה לשווק תרופות למחלות קשות וטיפולים בתאי גזע, לאחר הוכחת בטיחות הטיפולים ויעילותם הראשונית בלבד, וזאת כדי לאפשר לחולים סופניים לזכות לטיפולים בשלב מוקדם.
בעשורים האחרונים, חברות הפארמה הגדולות ריכזו את מאמציהן בעיקר בפיתוח תרופות למחלות נפוצות, שבהן הרווחיות גדולה יותר. מנגד, מחלות המוגדרות כמחלות יתום, שבהן מספר החולים נאמד במאות אלפים בודדים בארה"ב, נדחקו לצד ברמת המחקר והפיתוח, בעיקר משיקולים כלכליים.

ישראל נחשבת למרכז מוביל בחקר ה־ALS, עם מומחים בעלי שם עולמי בתחום, מרכזים רפואיים מובילים המטפלים בחולים ופיתוחים חדשניים להתמודדות והתגברות על המחלה. המוצר המוביל (AstroRx) של קדימהסטם, שנוסדה על ידי יוסי בן יוסף ופרופסור מישל רבל, מבוסס על מחקרים ב־ALS המעידים על תפקוד לקוי של תאי תמך במוח (אסטרוציטים) שמוביל לפגיעה בתאי העצב ובשרירים.
הטכנולוגיה של קדימהסטם מאפשרת ייצור תאי תמך בריאים שמוזרקים לנוזל חוט השדרה של המטופל, ובכך להאט את התקדמות המחלה ולשפר את איכות ותוחלת חיי החולים.
בונים על התקדים היפני
קדימהסטם מתכננת שהטיפול יינתן פעם או פעמיים בשנה, עובדה העשויה להוזיל מאוד את העלויות הרפואיות. בכוונת החברה להתחיל במהלך 2017 בניסוי ראשון בחולי ALS שייערך במחלקה הנוירולוגית של בית החולים הדסה עין כרם, בפיקוח משרד הבריאות ולאחר השלמת ההכנות הדרושות על־פי מתווה שתואם עם ה־FDA. אם הניסוי יצליח, מקווים בקדימהסטם כי תקדים הענקת האישור לתרופה היפנית שנוסתה מחוץ לארה"ב, יפעל לטובתה.
עתה נותר לראות רק אם החברה שכבר שרפה, כאמור, 100 מיליון שקל, תספיק למצוא תרופה ל־ALS לפני שקופת המזומנים שלה תתרוקן.





